Koffeincitrat: stimulerande (fullständig receptinformation)
Varumärke: Cafcit
Generiskt namn: koffeincitrat
Doseringsform: injektion
Koffeincitrat är ett stimulerande medel från centrala nervsystemet som finns som Cafcit, som används för att behandla apné hos spädbarn. Användning, dosering, biverkningar.
Innehåll:
Beskrivning
Klinisk farmakologi
Indikationer och användning
varningar
försiktighetsåtgärder
Negativa reaktioner
överdosering
Dosering och administrering
Hur levereras
Information om koffeincitrat (på vanligt engelska)
Beskrivning
Både koffeincitratinjektion för intravenös administrering och koffeincitrat oral lösning är klar, färglös, steril, icke-pyrogen, konserveringsfria vattenhaltiga lösningar justerade till pH 4.7. Varje ml innehåller 20 mg koffeincitrat (motsvarande 10 mg koffeinbas) framställt i lösning genom tillsats av 10 mg vattenfritt koffein, USP till 5 mg citronsyramonhydrat, USP, 8,3 mg natriumcitratdihydrat, USP och vatten för Injektion, USP.
Koffein, ett stimulerande medel i centrala nervsystemet, är ett luktfritt vitt kristallint pulver eller granulat med en bitter smak. Det är sparsamt lösligt i vatten och etanol vid rumstemperatur. Det kemiska namnet på koffein är 3,7-dihydro-1,3,7-trimetyl-1 H-purin-2,6-dion. I närvaro av citronsyra bildar den koffeincitratsalt i lösning. Strukturformeln och molekylvikten för koffeincitrat följer.
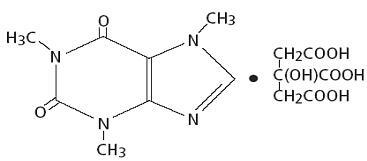
Koffeincitrat
C14H18N4O9 Mol. Vikt. 386,31
topp
Klinisk farmakologi
Handlingsmekanism
Koffein är strukturellt relaterat till andra metylxantiner, teofyllin och teobromin. Det är en slakmedelsavslappnande bronkial, en CNS-stimulant, en hjärtmuskelstimulant och ett diuretikum.
fortsätt historien nedan
Även om verkningsmekanismen för koffein i apné med för tidigt födsel inte är känd, har flera mekanismer antagits. Dessa inkluderar: (1) stimulering av andningscentret, (2) ökad minutventilation, (3) minskad tröskel till hyperkapnia, (4) ökat svar till hyperkapnia, (5) ökad skelettmuskelton, (6) minskad membranutmattning, (7) ökad metabolism och (8) ökad syre konsumtion.
De flesta av dessa effekter har tillskrivits antagonism av adenosinreceptorer, både A1- och A2-subtyper, av koffein, som har visats i receptorbindningsanalyser och observerats i koncentrationer ungefär de som uppnåtts terapeutiskt.
farmakokinetik
Absorption: Efter oral administrering av 10 mg koffeinbas / kg till för tidiga nyfödda är den maximala plasmanivån (Cmax) för koffein varierade från 6-10 mg / L och medeltiden för att uppnå toppkoncentration (Tmax) sträckte sig från 30 minuter till 2 timmar. Tmax påverkades inte av formelmatning. Den absoluta biotillgängligheten undersöktes emellertid inte helt hos förfödda nyfödda.
Distribution: koffein distribueras snabbt i hjärnan. Koffinnivåer i cerebrospinalvätskan hos för tidigt nyfödda ungefärliga deras plasmanivåer. Den genomsnittliga distributionen av koffein hos spädbarn (0,8-0,9 l / kg) är något högre än hos vuxna (0,6 l / kg). Plasmaproteinbindningsdata är inte tillgängliga för nyfödda eller spädbarn. Hos vuxna rapporteras den genomsnittliga plasmaproteinbindningen in vitro till cirka 36%.
Metabolism: Cytokrom P450 1A2 (CYP1A2) i lever är involverad i koffeinbiotransformation. Koffinmetabolism i för tidiga nyfödda är begränsad på grund av deras omogna leverenzymsystem.
Interkonversion mellan koffein och teofyllin har rapporterats hos förfödda nyfödda; koffeinnivåer är ungefär 25% av teofyllinnivåerna efter teofyllinadministration och cirka 3-8% av koffein som administreras förväntas konvertera till teofyllin.
Eliminering: Hos unga spädbarn är eliminering av koffein mycket långsammare än hos vuxna på grund av omogna lever- och / eller njurfunktioner. Genomsnittlig halveringstid (T1/2) och fraktion utsöndras oförändrad i urin (Ae) av koffein hos spädbarn har visats vara omvänt relaterat till graviditets- / postkonceptuell ålder. I nyfödda, T1/2 är ungefär 3-4 dagar och Ae är ungefär 86% (inom 6 dagar). Vid 9 månaders ålder ungefär är metabolism av koffein ungefär det som ses hos vuxna (T1/2 = 5 timmar och Ae = 1%).
Särskilda befolkningar: Studier som undersöker farmakokinetiken hos koffein hos nyfödda med nedsatt lever- eller njurfunktion har inte genomförts. Koffeincitrat bör administreras med försiktighet hos för tidigt nyfödda barn med nedsatt njur- eller leverfunktion. Serumkoncentrationer av koffein bör övervakas och dosadministrering av koffeincitrat bör justeras för att undvika toxicitet i denna population.
Kliniska studier
En multicenter, randomiserad, dubbelblind studie jämförde koffeincitrat med placebo hos åttiofem (85) förbarn (graviditetsålder 28 till <33 veckor) med apné av prematuritet. Apné med prematuritet definierades som att ha minst 6 apnepisoder av mer än 20 sekunder under en 24-timmarsperiod utan någon annan identifierbar orsak till apné. En 1 ml / kg (20 mg / kg koffeincitrat som gav 10 mg / kg som koffeinbas) belastningsdos av koffeincitrat administrerades intravenöst, följt av en 0,25 ml / kg (5 mg / kg koffeincitrat som tillhandahåller 2,5 mg / kg koffeinbas) daglig underhållsdos administrerad antingen intravenöst eller oralt (vanligtvis genom en utfodring rör). Behandlingstiden i denna studie var begränsad till 10 till 12 dagar. Protokollet tillät spädbarn att "räddas" med öppen etikett koffeincitratbehandling om deras apné förblev okontrollerad under den dubbelblinda fasen av försöket.
Andelen patienter utan apné på dag 2 av behandlingen (24-48 timmar efter laddningsdosen) var signifikant större med koffeincitrat än placebo. Följande tabell sammanfattar de kliniskt relevanta slutpunkterna utvärderade i denna studie: klipp
| Koffeincitrat | Placebo | p-värde | |
|---|---|---|---|
| Antal utvärderade patienter * | 45 | 37 | |
| % av patienterna med noll apnéhändelser dag 2 | 26.7 | 8.1 | 0.03 |
| Apnéfrekvens på dag 2 (per 24 timmar) | 4.9 | 7.2 | 0.134 |
| % av patienterna med 50% minskning av apnéhändelser från baslinjen på dag 2 | 76 | 57 | 0.07 |
| * Av 85 patienter som fick läkemedel, ingick inte 3 i effektivitetsanalysen eftersom de hade <6 apnepisoder / 24 timmar vid baslinjen. |
I denna 10-12-dagarsperiod var medelantalet dagar med noll apnéhändelser 3 i koffeincitratgruppen och 1,2 i placebogruppen. Det genomsnittliga antalet dagar med 50% minskning från baslinjen vid apnéhändelser var 6,8 i koffeincitratgruppen och 4,6 i placebogruppen.
topp
Indikationer och användning
Koffeincitratinjektion och koffeincitrat oral lösning är indicerade för kortvarig behandling av apné med för tidigt födsel hos barn mellan 28 och <33 veckors graviditetsålder.
topp
Kontra
Koffein citrat injektion och koffein citrat oral lösning är kontraindicerat hos patienter som har visat överkänslighet mot någon av dess komponenter.
topp
varningar
Under den dubbelblinda, placebokontrollerade kliniska prövningen utvecklades 6 fall av nekrotiserande enterokolit bland de 85 studerade spädbarn (koffein = 46, placebo = 39), med 3 fall som resulterade i dödsfall. Fem av de sex patienterna med nekrotiserande enterokolit randomiserades till eller hade utsatts för koffeincitrat.
Rapporter i den publicerade litteraturen har tagit upp en fråga om möjlig koppling mellan användning av metylxantiner och utveckling av nekrotiserande enterokolit, även om ett orsakssamband mellan metylxantinanvändning och nekrotiserande enterokolit inte har varit Etablerade. Därför bör patienter som behandlas med koffeincitrat noga övervakas noggrant för utvecklingen av nekrotiserande enterokolit.
topp
försiktighetsåtgärder
Allmän
Apné av förtid är en diagnos av uteslutning. Andra orsaker till apné (t.ex. störningar i centrala nervsystemet, primär lungsjukdom, anemi, sepsis, metaboliska störningar, kardiovaskulära avvikelser eller obstruktiv apné) bör uteslutas eller behandlas korrekt innan koffein påbörjas Citrat.
Koffein är en stimulant i centrala nervsystemet och i fall av överdosering av koffein har anfall rapporterats. Koffinsitrat bör användas med försiktighet hos spädbarn med krampanfall.
Behandlingstiden för apné med förtid i den placebokontrollerade studien var begränsad till 10 till 12 dagar. Säkerheten och effekten av koffeincitrat under längre behandlingsperioder har inte fastställts. Säkerhet och effekt av koffeincitrat för användning i profylaktisk behandling av plötslig spädbarnsdöd syndrom (SIDS) eller före extubation hos mekaniskt ventilerade spädbarn har inte heller varit det Etablerade.
hjärt
Även om inga fall av hjärttoxicitet rapporterades i den placebokontrollerade studien, har koffein visat sig öka hjärtfrekvensen, vänster ventrikulär produktion och slagvolym i publicerade studier. Därför bör koffeincitrat användas med försiktighet hos spädbarn med hjärt-kärlsjukdom.
Njursystem och leversystem
Koffinsitrat bör administreras med försiktighet hos spädbarn med nedsatt njur- eller leverfunktion. Serumkoncentrationer av koffein bör övervakas och dosadministrering av koffeincitrat bör justeras för att undvika toxicitet i denna population. (Ser Klinisk farmakologi, Eliminering, speciella befolkningar.)
Information för patienter
Föräldrar / vårdgivare för patienter som får koffeincitrat oral lösning bör få följande instruktioner:
- Caffeine Citrate oral lösning innehåller inga konserveringsmedel och varje injektionsflaska är endast för engångsbruk. Alla oanvända delar av medicinen bör kasseras.
- Det är viktigt att dosen av koffeincitrat oral lösning mäts noggrant, dvs med en 1 cc eller annan lämplig spruta.
- Kontakta din läkare om barnet fortsätter ha apnéhändelser; Öka inte dosen av koffeincitrat oral lösning utan medicinsk konsultation.
- Rådfråga din läkare om barnet börjar visa tecken på mag-tarmintolerans, såsom buksstörningar, kräkningar eller blodig avföring, eller om det verkar dött.
- Koffeinsitrat oral lösning bör inspekteras visuellt med avseende på partiklar och missfärgning innan den administreras. Injektionsflaskor som innehåller missfärgad lösning eller synliga partiklar bör kastas.
Laboratorietester
Innan koffeincitrat påbörjas bör serumnivåerna av koffein mätas i början spädbarn som tidigare behandlats med teofyllin, eftersom för tidigt spädbarn metaboliserar teofyllin till koffein. Likaså bör serumnivåer av koffein mätas hos spädbarn födda till mödrar som konsumerade koffein före leverans, eftersom koffein lätt korsar morkakan.
I den placebokontrollerade kliniska prövningen varierade koffeinnivåerna från 8 till 40 mg / l. Ett terapeutiskt plasmakoncentrationsområde för koffein kunde inte fastställas från den placebokontrollerade kliniska prövningen. Allvarlig toxicitet har rapporterats i litteraturen när koffeinhalten i serum överstiger 50 mg / L. Serumkoncentrationer av koffein kan behöva övervakas regelbundet under hela behandlingen för att undvika toxicitet.
I kliniska studier rapporterade i litteraturen har fall av hypoglykemi och hyperglykemi observerats. Därför kan serumglukos behöva kontrolleras regelbundet hos spädbarn som får koffeincitrat.
Läkemedelsinteraktioner
Cytokrom P450 1A2 (CYP1A2) är känt för att vara det huvudsakliga enzymet som är involverat i metabolismen av koffein. Därför har koffein potential att interagera med läkemedel som är substrat för CYP1A2, hämmar CYP1A2 eller inducerar CYP1A2.
Få data finns om läkemedelsinteraktioner med koffein hos förfödda nyfödda. Baserat på uppgifter om vuxna kan lägre doser koffein behövas efter samtidig administrering av läkemedel som rapporteras minska eliminering av koffein (t.ex. cimetidin och ketokonazol) och högre koffeindoser kan behövas efter samtidig administrering av läkemedel som ökar eliminering av koffein (t.ex. fenobarbital och fenytoin).
Koffin som administrerades samtidigt med ketoprofen minskade urinvolymen hos fyra friska frivilliga. Den kliniska betydelsen av denna interaktion hos prematura nyfödda är inte känd.
Interkonversion mellan koffein och teofyllin har rapporterats hos nyfödda nyfödda. Samtidig användning av dessa läkemedel rekommenderas inte.
Karcinogenes, mutagenes, nedsatt fertilitet
I en tvåårig studie på Sprague-Dawley-råttor var koffein (som koffeinbas) administrerat i dricksvatten inte cancerframkallande hos hanråttor i doser upp till 102 mg / kg eller hos honråttor i doser upp till 170 mg / kg (ungefär 2 respektive 4 gånger den maximala rekommenderade intravenösa belastningsdosen för spädbarn på en mg / m2 grund). I en 18-månadersstudie på C57BL / 6-möss sågs inga bevis på tumörgenicitet vid dietdoser upp till 55 mg / kg (mindre än den maximala rekommenderade intravenösa laddningsdosen för spädbarn på en mg / m2 grund).
Koffein (som koffeinbas) ökade systerkromatidutbytet (SCE) SCE / cellmetafas (exponeringstidsberoende) i en in vivo-metafasanalys av mus. Koffein förstärkte också genotoxiciteten hos kända mutagener och förstärkte mikronukleibildningen (5 gånger) hos möss med folatbrist. Koffein ökade emellertid inte kromosomavvikelser i äggstocksceller från kinesisk hamster in vitro (CHO) och humana lymfocytanalyser och var inte mutagen i en in vitro CHO / hypoxantin guanin fosforibosyltransferas (HGPRT) genmutationsanalys, utom vid cytotoxisk koncentrationer. Dessutom var koffein inte klastogent i en mikronukleusanalys in vivo.
Koffin (som koffeinbas) administreras till hanråttor med 50 mg / kg / dag subkutant (ungefär lika med den maximala rekommenderade intravenösa laddningsdosen för spädbarn på en mg / m2 bas) i 4 dagar före parning med obehandlade kvinnor, orsakade minskad reproduktionsprestanda för män utöver att orsaka embryotoxicitet. Dessutom var långvarig exponering för höga orala doser av koffein (3 g under sju veckor) giftig för råtta testiklar som manifesterades genom spermatogen celldegeneration.
Graviditet: Graviditet kategori C
Oro för koffeinens teratogenicitet är inte relevant när det ges till spädbarn. I studier utförda på vuxna djur, koffein (som koffeinbas) administreras till gravida möss som pellets med förlängd frisättning vid 50 mg / kg (mindre än den maximala rekommenderade intravenösa belastningsdosen för spädbarn på en mg / m2 under organogenesperioden, orsakade en låg förekomst av gomspalt och exencefali hos fostret. Det finns inga adekvata och välkontrollerade studier på gravida kvinnor.
topp
Negativa reaktioner
Sammantaget var det rapporterade antalet biverkningar under den dubbelblinda perioden i den kontrollerade studien liknande för koffeincitrat- och placebogrupperna. Följande tabell visar biverkningar som inträffade under den dubbelblinda perioden i den kontrollerade studien och som var vanligare hos patienter behandlade med koffeincitrat än placebo.
| Negativ händelse (AE) | Koffeincitrat N = 46 n (%) |
Placebo N = 39 n (%) |
|---|---|---|
| KROPP SOM HELT | ||
| Oavsiktlig skada | 1 (2.2) | 0 (0.0) |
| Matningsintolerans | 4 (8.7) | 2 (5.1) |
| Sepsis | 2 (4.3) | 0 (0.0) |
| KARDIOVASKULÄRA SYSTEMET | ||
| Blödning | 1 (2.2) | 0 (0.0) |
| MATSMÄLTNINGSSYSTEMET | ||
| Nekrotiserande enterokolit | 2 (4.3) | 1 (2.6) |
| Gastrit | 1 (2.2) | 0 (0.0) |
| Gastrointestinal blödning | 1 (2.2) | 0 (0.0) |
| HEMISKT OCH LYMFATISKT SYSTEM | ||
| Disseminerad intravaskulär koagulering | 1 (2.2) | 0 (0.0) |
| METABOLISKA OCH NUTRITIVA STÖD | ||
| acidos | 1 (2.2) | 0 (0.0) |
| Helande onormalt | 1 (2.2) | 0 (0.0) |
| NERVSYSTEM | ||
| Hjärnblödning | 1 (2.2) | 0 (0.0) |
| ANDNINGSSYSTEM | ||
| dyspné | 1 (2.2) | 0 (0.0) |
| Lungödem | 1 (2.2) | 0 (0.0) |
| HUD OCH TILLÄGG | ||
| Torr hud | 1 (2.2) | 0 (0.0) |
| Utslag | 4 (8.7) | 3 (7.7) |
| Huduppdelning | 1 (2.2) | 0 (0.0) |
| SÄRSKILDA SENSER | ||
| Retinopati av förfall | 1 (2.2) | 0 (0.0) |
| UROGENITAL SYSTEM | ||
| Njursvikt | 1 (2.2) | 0 (0.0) |
Förutom ovanstående fall diagnostiserades tre fall av nekrotiserande enterokolit hos patienter som fick koffeincitrat under den öppna etappen av studien.
Tre av spädbarn som utvecklade nekrotiserande enterokolit under rättegången dog. Alla hade utsatts för koffein. Två randomiserades till koffein, och en placebopatient "räddades" med öppen etikett koffein för okontrollerad apné.
Biverkningar som beskrivs i den publicerade litteraturen inkluderar: stimulering av centrala nervsystemet (dvs. irritabilitet, rastlöshet, jitteriness), kardiovaskulära effekter (d.v.s. takykardi, ökad vänster ventrikulär produktion och ökad slagvolym), gastrointestinala effekter (dvs. ökad gastrisk aspirat, gastrointestinal intolerans), förändringar i serumglukos (hypoglykemi och hyperglykemi) och njureffekter (ökat urinflöde, ökad kreatininclearance och ökad natrium och kalcium exkretion). Publicerade långsiktiga uppföljningsstudier har inte visat att koffein påverkar neurologisk utveckling eller tillväxtparametrar negativt.
topp
överdosering
Efter överdosering har koffeinhalten i serum varierat från cirka 24 mg / L (efter marknadsföring) spontan fallrapport där ett barn uppvisade irritabilitet, dålig utfodring och sömnlöshet) till 350 mg / L. Allvarlig toxicitet har associerats med serumnivåer mer än 50 mg / L (se försiktighetsåtgärder-Laboratoriska tester och Dosering och administrering). Tecken och symtom som rapporterats i litteraturen efter överdosering av koffein hos för tidigt födda barn inkluderar feber, takypné, jitteriness, sömnlöshet, fin tremor i extremiteterna, hypertoni, opisthotonos, tonisk-kloniska rörelser, otillräcklig käke- och läpprörelser, kräkningar, hyperglykemi, förhöjd urea-kväve i blodet och förhöjd total leukocyt koncentration. Beslag har också rapporterats i fall av överdosering. Ett fall av överdosering av koffein komplicerat av utveckling av intraventrikulär blödning och långvariga neurologiska följder har rapporterats. Ett annat fall av överdosering av koffeincitrat (från Nya Zeeland) av uppskattningsvis 600 mg koffeincitrat (ungefär 322 mg / kg) administrerat under 40 minuter komplicerade av takykardi, ST-depression, andningsbesvär, hjärtsvikt, magbesvär, acidos och en svår extravasationsförbränning med vävnadsnekros vid perifera intravenösa injektionsstället. Inga dödsfall i samband med överdosering av koffein har rapporterats hos för tidigt spädbarn.
Behandling av överdosering av koffein är främst symtomatisk och stödjande. Koffinnivåer har visat sig minska efter utbytetransfusioner. Kramper kan behandlas med intravenös administrering av diazepam eller ett barbiturat såsom pentobarbitalnatrium.
topp
Dosering och administrering
Innan koffeincitrat påbörjas bör serumnivåerna av koffein mätas i början spädbarn som tidigare behandlats med teofyllin, eftersom för tidigt spädbarn metaboliserar teofyllin till koffein. Likaså bör serumnivåer av koffein mätas hos spädbarn födda till mödrar som konsumerade koffein före leverans, eftersom koffein lätt korsar morkakan.
Den rekommenderade laddningsdosen och underhållsdoserna koffeincitrat följer.
| Dos av koffeincitrat Volym |
Dos av koffeincitrat mg / kg |
Rutt | Frekvens | |
|---|---|---|---|---|
| Laddar dos | 1 ml / kg | 20 mg / kg | Intravenös * (över 30 minuter) | En gång |
| Underhållsdos | 0,25 ml / kg | 5 mg / kg | Intravenöst * (över 10 minuter) eller muntligt | Var 24: e timme ** |
| * med en injektionspump för spruta ** börjar 24 timmar efter laddningsdosen |
OBSERVERA att dosen av koffeinbas är en hälften av dosen när den uttrycks som koffeincitrat (t.ex. 20 mg koffeincitrat motsvarar 10 mg koffeinbas).
Serumkoncentrationer av koffein kan behöva övervakas regelbundet under hela behandlingen för att undvika toxicitet. Allvarlig toxicitet har associerats med serumnivåer större än 50 mg / L.
Koffeincitratinjektion och koffeincitrat oral lösning bör inspekteras visuellt med avseende på partiklar och missfärgning före administrering. Injektionsflaskor som innehåller missfärgad lösning eller synliga partiklar bör kastas.
Läkemedelskompatibilitet
För att testa för läkemedelskompatibilitet med vanliga intravenösa lösningar eller mediciner, var 20 ml koffeincitratinjektion kombinerat med 20 ml av en lösning eller medicinering, med undantag av en Intralipid®-blandning, som kombinerades som 80 ml / 80 ml. Det fysiska utseendet på de kombinerade lösningarna utvärderades med avseende på utfällning. Blandningarna blandades i 10 minuter och analyserades sedan med avseende på koffein. Blandningarna blandades sedan kontinuerligt i 24 timmar, med ytterligare provtagning för koffeinanalyser vid 2, 4, 8 och 24 timmar.
Baserat på denna testning, koffeincitratinjektion, är 60 mg / 3 ml kemiskt stabilt under 24 timmar vid rumstemperatur i kombination med följande testprodukter.
- Dextrosinjektion, USP 5%
- 50% dextrosinjektion USP
- Intralipid® 20% IV fettemulsion
- Aminosyn® 8,5% kristallin aminosyralösning
- Dopamin HCI-injektion, USP 40 mg / ml utspädd till 0,6 mg / ml med Dextrosinjektion, USP 5%
- Kalciumglukonatinjektion, USP 10% (0,465 mEq / Ca + 2 / ml)
- Heparin natriuminjektion, USP 1000 enheter / ml utspädd till 1 enhet / ml med Dextrosinjektion, USP 5%
- Fentanylcitratinjektion, USP 50 | ig / ml utspädd till 10 | ig / ml med Dextrosinjektion, USP 5%
topp
Hur levereras
Både koffeincitratinjektion och koffeincitrat oral lösning finns som klara, färglösa, sterila, icke-pyrogena, konserveringsfria, vattenhaltiga lösningar i 5 ml färglösa glasflaskor. Injektionsflaskorna med koffeincitratinjektion är förseglade med grått gummipropp och vitt aluminiumtätning tryckt med "FÖR INTRAVENöst användning" i rött. Injektionsflaskorna med koffeincitrat oral lösning är förseglade med grått gummipropp och en mörkblå matt finish, vippa av rivning av aluminiumtätning tryckt med "FÖR ORAL ANVÄNDNING - FLIP UP & TEAR" in vit.
Både injektionsflaskorna med injektion och oral lösning innehåller 3 ml lösning i en koncentration av 20 mg / ml koffeincitrat (60 mg / flaska) motsvarande 10 mg / ml koffeinbas (30 mg / flaska).
Koffeinsitratinjektion, USP
NDC 47335-289-40: 3 ml injektionsflaska, individuellt förpackad i en kartong.
Koffeinsitrat oral lösning, USP
NDC 47335-290-44: 3 ml injektionsflaska (INTE BARNBESTAND), 10 injektionsflaskor per vit
barnsäker behållare av polypropen.
Förvara vid 20 till 25 ° C (68 ° till 77 ° F); utflykter tillåtna mellan 15 ° och 30 ° C (59 ° och 86 ° F) [se USP-kontrollerad rumstemperatur].
Konserveringsmedel gratis. Endast för engångsbruk. Kassera oanvänd del.
ATTENTION PHARMACIST: Ta bort "bruksanvisning" från förpackningen och skicka ut recept på koffeincitrat oral lösning.
Levererad av:
Caraco Pharmaceutical Laboratories, Ltd.
1150 Elijah McCoy Drive, Detroit, MI 48202
Tillverkad av:
Sun Pharmaceutical Ind. Ltd.
Halol-Baroda Highway,
Halol-389 350, Gujarat, Indien.
senast uppdaterad 02/2010
Information om koffeincitrat (på vanligt engelska)
Detaljerad information om Tecken, symtom, orsaker, behandling av sömnstörningar
Informationen i denna monografi är inte avsedd att täcka alla möjliga användningar, anvisningar, försiktighetsåtgärder, läkemedelsinteraktioner eller negativa effekter. Denna information är generaliserad och är inte avsedd som specifik medicinsk rådgivning. Om du har frågor om läkemedlen du tar eller vill ha mer information, kontakta din läkare, apotekspersonal eller sjuksköterska.
tillbaka till:
~ alla artiklar om sömnstörningar



