Lantus för behandling av diabetes
Varumärke: Lantus
Generiskt namn: insulin glargine
Doseringsform: Injektion (Lantus får INTE spädas eller blandas med något annat insulin eller lösning)
Innehåll:
Beskrivning
Klinisk farmakologi
Indikationer och användning
Kontra
varningar
försiktighetsåtgärder
Negativa reaktioner
Dosering och administrering
Hur levereras
Lantus, insulin glargin (rDNA-ursprung), patientinformation (på vanligt engelska)
Beskrivning
Lantus® (insulin glargine [rDNA origin] -injektion) är en steril lösning av insulin glargine för användning som injektion. Insulin glargin är en rekombinant humaninsulinanalog som är en långverkande (upp till 24-timmars verkningsperiod), parenteralt blodsockersänkande medel. (Ser KLINISK FARMAKOLOGI). Lantus produceras genom rekombinant DNA-teknik med användning av en icke-patogen laboratoriestam av Escherichia coli (K12) som produktionsorganism. Glarginsulin skiljer sig från humant insulin genom att aminosyran asparagin i position A21 ersätts av glycin och två argininer tillsätts till C-terminalen i B-kedjan. Kemiskt är det 21A-Gly-30Ba-L-Arg-30Bb-L-Arg-humant insulin och har den empiriska formeln C267H404N72O78S6 och en molekylvikt av 6063. Den har följande strukturformel:
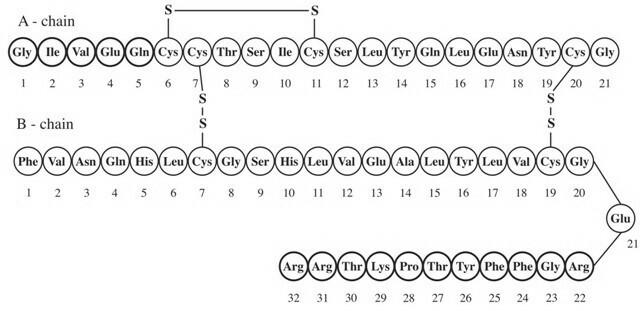
Lantus består av insulin glargin upplöst i en klar vattenhaltig vätska. Varje milliliter Lantus (insulin glargin injektion) innehåller 100 IE (3,6378 mg) insulin glargine.
Inaktiva ingredienser för 10 ml injektionsflaskan är 30 mcg zink, 2,7 mg m-cresol, 20 mg glycerol 85%, 20 mcg polysorbat 20 och vatten för injektion.
Inaktiva ingredienser för 3 ml patronen är 30 mcg zink, 2,7 mg m-cresol, 20 mg glycerol 85% och vatten för injektion.
PH justeras genom tillsats av vattenhaltiga lösningar av saltsyra och natriumhydroxid. Lantus har ett pH av cirka 4.
topp
Klinisk farmakologi
Handlingsmekanism
Den primära aktiviteten för insulin, inklusive insulin glargin, är reglering av glukosmetabolismen. Insulin och dess analoger sänker blodglukosnivåerna genom att stimulera perifert glukosupptag, speciellt genom skelettmuskulatur och fett, och genom att hämma glukosproduktion i lever. Insulin hämmar lipolys i adipocyten, hämmar proteolys och förbättrar proteinsyntesen.
farmakodynamik
Insulin glargin är en human insulinanalog som har utformats för att ha låg vattenlöslighet vid neutralt pH. Vid pH 4, som i Lantus-injektionslösningen, är den fullständigt löslig. Efter injektion i den subkutana vävnaden neutraliseras den sura lösningen vilket leder till bildning av mikroutfällningar från vilka små mängder insulin glargin frigörs långsamt, vilket resulterar i en relativt konstant koncentration / tidsprofil under 24 timmar utan uttalat topp. Denna profil tillåter dosering en gång dagligen som en patients basalinsulin.
I kliniska studier är den glukosreducerande effekten på molär basis (dvs när den ges vid samma doser) av intravenös insulin glargin ungefär densamma som humant insulin. I euglykemiska klämstudier på friska personer eller hos patienter med typ 1-diabetes var effekten av subkutan glargininsats långsammare än NPH-humant insulin. Effektprofilen för insulin glargin var relativt konstant utan uttalad topp och varaktigheten av dess effekt var förlängd jämfört med NPH humant insulin. Figur 1 visar resultat från en studie på patienter med typ 1-diabetes utförd i högst 24 timmar efter injektionen. Mediantiden mellan injektion och slutet av den farmakologiska effekten var 14,5 timmar (intervall: 9,5 till 19,3 timmar) för NPH humant insulin och 24 timmar (intervall: 10,8 till> 24,0 timmar) (24 timmar var slutet av observationsperioden) för insulin glargin.
Figur 1. Aktivitetsprofil hos patienter med typ 1-diabetes?

* Bestämd som mängd glukos infunderad för att upprätthålla konstanta plasmaglukosnivåer (medelvärden per timme); indikerar insulinaktivitet.
â € mellan patientens variation (CV, variationskoefficient); insulin glargin, 84% och NPH, 78%.
Den längre verkningstiden (upp till 24 timmar) av Lantus är direkt relaterad till dess långsammare absorptionshastighet och stöder subkutan administrering en gång dagligen. Tidsförloppet för insuliner, inklusive Lantus, kan variera mellan individer och / eller inom samma individ.
farmakokinetik
Absorption och biotillgänglighet
Efter subkutan injektion av insulin glargine hos friska personer och hos patienter med diabetes indikerade insulinserumkoncentrationerna a långsammare, mer långvarig absorption och en relativt konstant koncentration / tidsprofil under 24 timmar utan uttalad topp i jämförelse med NPH-människa insulin. Seruminsulinkoncentrationer var således förenliga med tidsprofilen för den farmakodynamiska aktiviteten hos glarginsulin.
Efter subkutan injektion av 0,3 IE / kg insulin glargin hos patienter med typ 1-diabetes har en relativt konstant koncentration / tidsprofil visats. Verkningstiden efter subkutan administrering av buken, deltoid eller låret var likadan.
Ämnesomsättning
En metabolismstudie hos människor indikerar att insulin glargin delvis metaboliseras vid karboxylterminalen i B-kedjan i den subkutana depå för att bilda två aktiva metaboliter med in vitro-aktivitet liknande den för insulin, M1 (21A-Gly-insulin) och M2 (21A-Gly-des-30B-Thr-insulin). Oförändrat läkemedel och dessa nedbrytningsprodukter finns också i cirkulationen.
Särskilda befolkningar
Ålder, ras och kön
Information om effekten av ålder, ras och kön på Lantus farmakokinetik är inte tillgänglig. I kontrollerade kliniska prövningar hos vuxna (n = 3890) och en kontrollerad klinisk prövning hos pediatriska patienter (n = 349) var dock subgrupp analyser baserade på ålder, ras och kön visade inte skillnader i säkerhet och effekt mellan insulin glargin och NPH-människa insulin.
Rökning
Effekten av rökning på Lantus farmakokinetik / farmakodynamik har inte studerats.
Graviditet
Effekten av graviditet på farmakokinetiken och farmakodynamiken hos Lantus har inte studerats (se FÖRSIKTIGHETSÅTGÄRDER, Graviditet).
Fetma
I kontrollerade kliniska studier, som inkluderade patienter med Body Mass Index (BMI) upp till och med 49,6 kg / m2, undergruppsanalyser baserade på BMI visade inga skillnader i säkerhet och effekt mellan insulin glargin och NPH-människa insulin.
Nedsatt njurfunktion
Effekten av nedsatt njurfunktion på Lantus farmakokinetik har inte studerats. Vissa studier med humant insulin har emellertid visat ökade cirkulationsnivåer av insulin hos patienter med njursvikt. Noggrann glukosövervakning och dosjustering av insulin, inklusive Lantus, kan vara nödvändig hos patienter med nedsatt njurfunktion (se FÖRSIKTIGHETSÅTGÄRDER, Nedsatt njurfunktion).
Nedsatt leverfunktion
Effekten av nedsatt leverfunktion på Lantus farmakokinetik har inte studerats. Vissa studier med humant insulin har emellertid visat ökade cirkulationsnivåer av insulin hos patienter med leversvikt. Noggrann glukosövervakning och dosjustering av insulin, inklusive Lantus, kan vara nödvändigt hos patienter med leverdysfunktion (se FÖRSIKTIGHETSÅTGÄRDER, Nedsatt leverfunktion).
Kliniska studier
Säkerheten och effektiviteten för insulin glargin som ges en gång dagligen vid sänggåendet jämfördes med den för human insulin insulin en gång dagligen och två gånger dagligen i öppet, randomiserat, aktiv kontroll, parallella studier av 2327 vuxna patienter och 349 pediatriska patienter med typ 1-diabetes mellitus och 1563 vuxna patienter med typ 2-diabetes mellitus (se tabeller 1-3). I allmänhet var reduktionen i glycerat hemoglobin (HbA1c) med Lantus liknande den med NPH humant insulin. De totala nivåerna av hypoglykemi skilde sig inte mellan patienter med diabetes som behandlades med Lantus jämfört med NPH humant insulin.
Diabetes-vuxen av typ 1 (se tabell 1).
I två stora, slumpmässiga, kontrollerade kliniska studier (studier A och B), patienter med typ 1-diabetes (studie A; n = 585, studie B; n = 534) randomiserades till basal-bolusbehandling med Lantus en gång dagligen vid sänggåendet eller till NPH humant insulin en eller två gånger dagligen och behandlades under 28 veckor. Regelbundet humant insulin administrerades före varje måltid. Lantus administrerades vid sänggåendet. NPH humant insulin administrerades en gång dagligen vid sänggåendet eller på morgonen och vid sänggåendet vid användning två gånger dagligen. I en stor, randomiserad, kontrollerad klinisk studie (studie C), patienter med typ 1-diabetes (n = 619) behandlades i 16 veckor med en basal-bolus insulinregim där insulin lispro användes före varje måltid. Lantus administrerades en gång dagligen vid sänggåendet och NPH humant insulin administrerades en eller två gånger dagligen. I dessa studier hade Lantus och NPH humant insulin en liknande effekt på glykohemoglobin med en liknande total hastighet av hypoglykemi.
Tabell 1: Typ 1 Diabetes Mellitus-Adult
| Studie A | Studie B | Studie C | ||||
|---|---|---|---|---|---|---|
| Behandlingstid | 28 veckor | 28 veckor | 16 veckor | |||
| Behandling i kombination med | Vanlig insulin | Vanlig insulin | Insulin lispro | |||
| Lantus | NPH | Lantus | NPH | Lantus | NPH | |
| Antal behandlade personer | 292 | 293 | 264 | 270 | 310 | 309 |
| HbA1c | ||||||
| Endstudie medelvärde | 8.13 | 8.07 | 7.55 | 7.49 | 7.53 | 7.60 |
| Adj. genomsnittlig förändring från baslinjen | +0.21 | +0.10 | -0.16 | -0.21 | -0.07 | -0.08 |
| Lantus - NPH | +0.11 | +0.05 | +0.01 | |||
| 95% CI för behandlingsskillnad | (-0.03; +0.24) | (-0.08; +0.19) | (-0.11; +0.13) | |||
| Basal insulindos | ||||||
| Endstudie medelvärde | 19.2 | 22.8 | 24.8 | 31.3 | 23.9 | 29.2 |
| Genomsnittlig förändring från baslinjen | -1.7 | -0.3 | -4.1 | +1.8 | -4.5 | +0.9 |
| Total insulindos | ||||||
| Endstudie medelvärde | 46.7 | 51.7 | 50.3 | 54.8 | 47.4 | 50.7 |
| Genomsnittlig förändring från baslinjen | -1.1 | -0.1 | +0.3 | +3.7 | -2.9 | +0.3 |
| Fastande blodsocker (mg / dL) | ||||||
| Endstudie medelvärde | 146.3 | 150.8 | 147.8 | 154.4 | 144.4 | 161.3 |
| Adj. genomsnittlig förändring från baslinjen | -21.1 | -16.0 | -20.2 | -16.9 | -29.3 | -11.9 |
Diabetes-pediatrisk typ 1 (se tabell 2).
I en randomiserad, kontrollerad klinisk studie (studie D), pediatriska patienter (åldersintervallet 6 till 15 år) med typ 1-diabetes (n = 349) behandlades under 28 veckor med en basal-bolus insulinregim där vanligt humant insulin användes före varje måltid. Lantus administrerades en gång dagligen vid sänggåendet och NPH humant insulin administrerades en eller två gånger dagligen. Liknande effekter på glykohemoglobin och förekomsten av hypoglykemi observerades i båda behandlingsgrupperna.
Tabell 2: Typ 1 Diabetes Mellitus-Pediatric
| Studie D | ||
|---|---|---|
| Behandlingstid | 28 veckor | |
| Behandling i kombination med | Vanlig insulin | |
| Lantus | NPH | |
| Antal behandlade personer | 174 | 175 |
| HbA1c | ||
| Endstudie medelvärde | 8.91 | 9.18 |
| Adj. genomsnittlig förändring från baslinjen | +0.28 | +0.27 |
| Lantus - NPH | +0.01 | |
| 95% CI för behandlingsskillnad | (-0.24; +0.26) | |
| Basal insulindos | ||
| Endstudie medelvärde | 18.2 | 21.1 |
| Genomsnittlig förändring från baslinjen | -1.3 | +2.4 |
| Total insulindos | ||
| Endstudie medelvärde | 45.0 | 46.0 |
| Genomsnittlig förändring från baslinjen | +1.9 | +3.4 |
| Fastande blodsocker (mg / dL) | ||
| Endstudie medelvärde | 171.9 | 182.7 |
| Adj. genomsnittlig förändring från baslinjen | -23.2 | -12.2 |
Diabetes-vuxen av typ 2 (se tabell 3).
I en stor, slumpmässig, kontrollerad klinisk studie (studie E) (n = 570) utvärderades Lantus under 52 veckor som en del av ett kombinationsterapi med insulin och orala antidiabetesmedel (en sulfonylurea, metformin, akarbos eller kombinationer av dessa läkemedel). Lantus som administrerades en gång dagligen vid sänggåendet var lika effektiv som NPH humant insulin som administrerades en gång dagligen vid sänggåendet för att minska glykohemoglobin och fasta glukos. Det fanns en låg hastighet av hypoglykemi som var likadan hos Lantus- och NPH-mänskliga insulinbehandlade patienter. I en stor, slumpmässig, kontrollerad klinisk studie (studie F), hos patienter med typ 2-diabetes som inte använder orala antidiabetesmedel (n = 518), en basal-bolusregim av Lantus en gång dagligen vid sänggåendet eller NPH humant insulin administrerat en eller två gånger dagligen utvärderades för 28 veckor. Vanligt humant insulin användes före måltid efter behov. Lantus hade liknande effektivitet som antingen en eller två gånger dagligen NPH humant insulin för att minska glykohemoglobin och fasta glukos med en liknande förekomst av hypoglykemi.
Tabell 3: Typ 2-diabetes mellitus-adult
| Studie E | Studie F | |||
|---|---|---|---|---|
| Behandlingstid | 52 veckor | 28 veckor | ||
| Behandling i kombination med | Orala medel | Vanlig insulin | ||
| Lantus | NPH | Lantus | NPH | |
| Antal behandlade personer | 289 | 281 | 259 | 259 |
| HbA1c | ||||
| Endstudie medelvärde | 8.51 | 8.47 | 8.14 | 7.96 |
| Adj. genomsnittlig förändring från baslinjen | -0.46 | -0.38 | -0.41 | -0.59 |
| Lantus - NPH | -0.08 | +0.17 | ||
| 95% CI för behandlingsskillnad | (-0.28; +0.12) | (-0.00; +0.35) | ||
| Basal insulindos | ||||
| Endstudie medelvärde | 25.9 | 23.6 | 42.9 | 52.5 |
| Genomsnittlig förändring från baslinjen | +11.5 | +9.0 | -1.2 | +7.0 |
| Total insulindos | ||||
| Endstudie medelvärde | 25.9 | 23.6 | 74.3 | 80.0 |
| Genomsnittlig förändring från baslinjen | +11.5 | +9.0 | +10.0 | +13.1 |
| Fastande blodsocker (mg / dL) | ||||
| Endstudie medelvärde | 126.9 | 129.4 | 141.5 | 144.5 |
| Adj. genomsnittlig förändring från baslinjen | -49.0 | -46.3 | -23.8 | -21.6 |
Lantus flexibel daglig dosering
Säkerheten och effekten av Lantus administrerad före frukost, före middagen eller vid sänggåendet var utvärderades i en stor, randomiserad, kontrollerad klinisk studie, hos patienter med typ 1-diabetes (studie G, n = 378). Patienterna behandlades också med insulin lispro vid måltiden. Lantus som administrerades vid olika tidpunkter på dagen resulterade i liknande minskningar av glycerat hemoglobin jämfört med det vid administrering vid sänggåendet (se tabell 4). Hos dessa patienter finns data tillgängliga från 8-punkts hemglukosövervakning. Den maximala genomsnittliga blodglukosnivån observerades strax före injektion av Lantus oavsett administreringstid, dvs före frukost, förmiddag eller sänggåendet.
I denna studie avbröt 5% av patienterna i Lantus-frukostarmen behandlingen på grund av bristande effekt. Inga patienter i de andra två armarna avbröts av detta skäl. Rutinmässig övervakning under denna studie avslöjade följande medelförändringar i systoliskt blodtryck: grupp före frukost, 1,9 mm Hg; grupp för middag, 0,7 mm Hg; grupp före sänggåendet, -2,0 mm Hg.
Säkerheten och effekten av Lantus administrerad före frukost eller vid läggdags utvärderades också i en stor, slumpmässig, aktivt kontrollerad klinisk studie (studie H, n = 697) hos patienter av typ 2-diabetes som inte längre var tillräckligt kontrollerade på oralt medel terapi. Alla patienter i denna studie fick också AMARYL® (glimepirid) 3 mg dagligen. Lantus som givits före frukosten var minst lika effektiv för att sänka glykerat hemoglobin A1c (HbA1c) som Lantus ges vid sänggåendet eller NPH humant insulin som gavs vid sänggåendet (se tabell 4).
Tabell 4: Flexibel Lantus daglig dosering i typ 1 (studie G) och typ 2 (studie H) Diabetes Mellitus
| Studie G | Studie H | |||||
|---|---|---|---|---|---|---|
| Treatmentduration | 24 veckor | 24 veckor | ||||
| Behandling i kombination med: | Insulin lispro | AMARYL® (glimepiride) | ||||
| Lantus Frukost |
Lantus Middag |
Lantus Bedtime |
Lantus Frukost |
Lantus Bedtime |
NPH Bedtime |
|
| ||||||
| Antal behandlade personer* | 112 | 124 | 128 | 234 | 226 | 227 |
| HbA1c | ||||||
| Basvärde | 7.56 | 7.53 | 7.61 | 9.13 | 9.07 | 9.09 |
| Endstudie medelvärde | 7.39 | 7.42 | 7.57 | 7.87 | 8.12 | 8.27 |
| Genomsnittlig förändring från baslinjen | -0.17 | -0.11 | -0.04 | -1.26 | -0.95 | -0.83 |
| Basal insulindos (IU) | ||||||
| Endstudie medelvärde | 27.3 | 24.6 | 22.8 | 40.4 | 38.5 | 36.8 |
| Genomsnittlig förändring från baslinjen | 5.0 | 1.8 | 1.5 | |||
| Total insulindos (IU) | Naa € | NA | NA | |||
| Endstudie medelvärde | 53.3 | 54.7 | 51.5 | |||
| Genomsnittlig förändring från baslinjen | 1.6 | 3.0 | 2.3 |
topp
Indikationer och användning
Lantus är indicerat för subkutan administrering en gång dagligen för behandling av vuxna och pediatriska patienter med typ 1 diabetes mellitus eller vuxna patienter med typ 2 diabetes mellitus som behöver basal (långverkande) insulin för kontroll av hyperglykemi.
topp
Kontra
Lantus är kontraindicerat hos patienter som är överkänsliga för glarginsulin eller hjälpämnen.
topp
varningar
Hypoglykemi är den vanligaste biverkningen av insulin, inklusive Lantus. Som med alla insuliner kan tidpunkten för hypoglykemi variera mellan olika insulinformuleringar. Glukosövervakning rekommenderas för alla patienter med diabetes.
Alla förändringar av insulin bör göras försiktigt och endast under medicinsk övervakning. Förändringar i insulinstyrka, doseringstid, tillverkare, typ (t.ex. vanliga, NPH- eller insulinanaloger), arter (djur, människa) eller tillverkningsmetod (rekombinant DNA kontra djurinsulininsulin) kan leda till behovet av en förändring i dosering. Samtidig oral behandling med antidiabetes kan behöva justeras.
topp
försiktighetsåtgärder
Allmän
Lantus är inte avsett för intravenös administrering. Den förlängda aktivitetsperioden för insulin glargin är beroende av injektion i subkutan vävnad. Intravenös administrering av den vanliga subkutana dosen kan leda till svår hypoglykemi.
Lantus får INTE spädas eller blandas med något annat insulin eller lösning. Om Lantus är utspädd eller blandad kan lösningen bli grumlig och den farmakokinetiska / farmakodynamiska profilen (t.ex. början av verkan, tid till toppeffekt) av Lantus och / eller det blandade insulinet kan förändras i en oförutsägbar sätt. När Lantus och vanligt humant insulin blandades omedelbart före injektion hos hundar, observerades en försenad insats och tid till maximal effekt för vanlig humant insulin. Blandningens totala biotillgänglighet minskade också något jämfört med separata injektioner av Lantus och vanligt humant insulin. Relevansen av dessa observationer hos hundar för människor är inte känd.
Liksom med alla insulinpreparat kan Lantus-åtgärdens tid variera i olika individer eller på olika sätt gånger hos samma individ och absorptionshastigheten är beroende av blodtillförsel, temperatur och fysisk aktivitet.
Insulin kan orsaka natriumretention och ödem, särskilt om tidigare dålig metabolisk kontroll förbättras genom intensifierad insulinbehandling.
hypoglykemi
Som med alla insulinpreparat kan hypoglykemiska reaktioner vara associerade med administreringen av Lantus. Hypoglykemi är den vanligaste negativa effekten av insuliner. Tidiga varningssymptom på hypoglykemi kan vara annorlunda eller mindre uttalade under vissa förhållanden, till exempel länge varaktighet av diabetes, diabetes nervsjukdom, användning av mediciner såsom betablockerare eller intensifierad diabeteskontroll (ser FÖRSIKTIGHETSÅTGÄRDER, Läkemedelsinteraktioner). Sådana situationer kan leda till svår hypoglykemi (och möjligen förlust av medvetande) innan patienternas medvetenhet om hypoglykemi.
Tidpunkten för förekomst av hypoglykemi beror på handlingsprofilen för de använda insulinerna och kan därför ändras när behandlingsregimen eller doseringstiden ändras. Patienter som byts från NPH-insulin två gånger dagligen till Lantus en gång dagligen bör ha initialt Lantus-dosen minskade med 20% från föregående total dagliga NPH-dos för att minska risken för hypoglykemi (ser DOSERING OCH ADMINISTRERING, Byte till Lantus).
Den långvariga effekten av subkutan Lantus kan försena återhämtningen från hypoglykemi.
I en klinisk studie var symtomen på hypoglykemi eller motreglerande hormonsvar liknande efter intravenöst glargint insulin och vanligt humant insulin både hos friska personer och patienter med typ 1 diabetes.
Nedsatt njurfunktion
Även om studier inte har utförts på patienter med diabetes och nedsatt njurfunktion, kräver Lantus kan minskas på grund av minskad insulinmetabolism, liknande observationer som hittades med andra insuliner (ser KLINISK FARMAKOLOGI, Speciella befolkningar).
Nedsatt leverfunktion
Även om studier inte har utförts på patienter med diabetes och nedsatt leverfunktion kan Lantuskraven minskas på grund av minskad kapacitet för glukoneogenes och minskad insulinmetabolism, liknande observationer som hittades med andra insuliner (se KLINISK FARMAKOLOGI, Speciella befolkningar).
Injektionsplats och allergiska reaktioner
Liksom med någon insulinbehandling kan lipodystrofi uppstå på injektionsstället och försena insulinabsorptionen. Andra reaktioner på injektionsstället med insulinbehandling inkluderar rodnad, smärta, klåda, nässelfeber, svullnad och inflammation. Kontinuerlig rotation av injektionsstället inom ett givet område kan bidra till att minska eller förhindra dessa reaktioner. De flesta mindre reaktioner på insuliner löper vanligtvis på några dagar till några veckor.
Rapporter om smärta på injektionsstället var oftare med Lantus än NPH humant insulin (2,7% glargint insulin mot 0,7% NPH). Rapporteringen om smärta på injektionsstället var vanligtvis milda och ledde inte till att behandlingen avbröts.
Allergiska reaktioner av omedelbar typ är sällsynta. Sådana reaktioner på insulin (inklusive insulin glargin) eller hjälpämnen kan till exempel vara associerade med generaliserade hudreaktioner, angioödem, bronkospasm, hypotension eller chock och kan vara liv hotfull.
Samtidiga förhållanden
Insulinbehov kan förändras under samtidiga tillstånd som sjukdom, känslomässiga störningar eller stress.
Information för patienter
Lantus får endast användas om lösningen är klar och färglös utan synliga partiklar (se DOSERING OCH ADMINISTRERING, Förberedelser och hantering).
Patienter måste informeras om att Lantus INTE får spädas eller blandas med något annat insulin eller lösning (se FÖRSIKTIGHETSÅTGÄRDER, Allmänt).
Patienterna bör instrueras om självhanteringsprocedurer inklusive glukosövervakning, korrekt injektionsteknik och hypoglykemi och hyperglykemihantering. Patienter måste instrueras om hantering av speciella situationer som till exempel strömförhållanden (sjukdom, stress eller känslomässig) störningar), en otillräcklig eller överhoppad insulindos, oavsiktlig administrering av en ökad insulindos, otillräckligt matintag, eller hoppade måltider. Se patienter i Lantus-cirkulären "Patientinformation" för ytterligare information.
Liksom för alla patienter som har diabetes kan förmågan att koncentrera sig och / eller reagera försämras till följd av hypoglykemi eller hyperglykemi.
Patienter med diabetes bör uppmanas att informera sin vårdpersonal om de är gravida eller överväger graviditet.
Läkemedelsinteraktioner
Ett antal ämnen påverkar glukosmetabolismen och kan kräva justering av insulindos och särskilt noggrann övervakning.
Följande är exempel på ämnen som kan öka den blodsockersänkande effekten och känsligheten för hypoglykemi: orala antidiabetesprodukter, ACE-hämmare, disopyramid, fibrater, fluoxetin, MAO-hämmare, propoxifen, salicylater, somatostatinanalog (t.ex. oktreotid), sulfonamid antibiotika.
Följande är exempel på ämnen som kan minska den blodsockersänkande effekten av insulin: kortikosteroider, danazol, diuretika, sympatomimetiska medel (t.ex. epinefrin, albuterol, terbutalin), isoniazid, fenotiazinderivat, somatropin, sköldkörtelhormoner, östrogener, progestogener (t.ex. i p-piller), proteashämmare och atypiska antipsykotiska läkemedel (t.ex. olanzapin och klozapin).
Betablockerare, klonidin, litiumsalter och alkohol kan antingen förstärka eller försvaga insulinets blodsockersänkande effekt. Pentamidin kan orsaka hypoglykemi, som ibland kan följas av hyperglykemi.
Dessutom, under påverkan av sympatolytiska läkemedel såsom betablockerare, klonidin, guanetidin och reserpin, kan tecknen på hypoglykemi reduceras eller saknas.
Karcinogenes, mutagenes, nedsatt fertilitet
Hos möss och råttor utfördes tvååriga karcinogenicitetsstudier med insulin glargin i doser upp till 0,455 mg / kg, vilket är för råtta ungefär 10 gånger och för musen ungefär 5 gånger den rekommenderade, subkutana startdosen för människa på 10 IE (0,008 mg / kg / dag), baserat på mg / m2. Resultaten hos kvinnliga möss var inte avgörande på grund av överdriven dödlighet i alla dosgrupper under studien. Histiocytomer hittades på injektionsställen hos hanråttor (statistiskt signifikanta) och hanmöss (inte statistiskt signifikanta) i sura bärare innehållande grupper. Dessa tumörer hittades inte i kvinnliga djur, i saltlösningskontroll eller insulinkomparatorgrupper med användning av en annan vehikel. Relevansen av dessa fynd för människor är okänd.
Glargininsulin var inte mutagent i tester för detektion av genmutationer i bakterier och däggdjursceller (Ames- och HGPRT-test) och i tester för detektion av kromosomavvikelser (cytogenetik in vitro i V79-celler och in vivo på kinesiska hamstrar).
I en kombinerad fertilitets- och prenatal och postnatal studie på han- och honråttor vid subkutana doser upp till 0,36 mg / kg / dag, vilket är ungefär 7 gånger rekommenderad subkutan startdos på 10 IE (0,008 mg / kg / dag), baserat på mg / m2, toxicitet hos mödrar på grund av dosberoende hypoglykemi, inklusive vissa dödsfall, var observeras. Följaktligen inträffade en minskning av uppfödningshastigheten endast i högdosgruppen. Liknande effekter observerades med humant NPH-insulin.
Graviditet
Teratogena effekter
Graviditet kategori C. Subkutan reproduktion och teratologistudier har utförts med glargininsulin och vanligt humant insulin hos råttor och Himalaya-kaniner. Läkemedlet gavs honråttor innan parning, under parning och under hela graviditeten i doser upp till 0,36 mg / kg / dag, vilket är ungefär 7 gånger den rekommenderade subkutana startdosen på 10 IE (0,008 mg / kg / dag), baserat på mg / m2. Hos kaniner är doser på 0,072 mg / kg / dag, vilket är ungefär två gånger den rekommenderade människan subkutan startdos på 10 IE (0,008 mg / kg / dag), baserat på mg / m2, administrerades under organogenes. Effekterna av insulin glargin skilde sig generellt inte från de som observerades med vanlig humant insulin hos råttor eller kaniner. Hos kaniner uppvisade emellertid fem fostrar från två kullar i högdosgruppen utvidgning av hjärnventriklarna. Fertilitet och tidig embryonal utveckling verkade normal.
Det finns inga välkontrollerade kliniska studier av användning av insulin glargin hos gravida kvinnor. Det är viktigt för patienter med diabetes eller en historia med graviditetsdiabetes att upprätthålla god metabolisk kontroll före befruktningen och under hela graviditeten. Insulinbehovet kan minska under första trimestern, öka i allmänhet under andra och tredje trimestern och minska snabbt efter förlossningen. Noggrann övervakning av glukoskontroll är nödvändig hos sådana patienter. Eftersom studier på reproduktion av djur inte alltid förutsäger människors svar, bör detta läkemedel användas under graviditet om det är klart nödvändigt.
Ammande mödrar
Det är okänt om glargininsulin utsöndras i betydande mängder i bröstmjölk. Många läkemedel, inklusive humant insulin, utsöndras i bröstmjölk. Av denna anledning bör försiktighet iakttas när Lantus ges till en ammande kvinna. Amningskvinnor kan behöva justeringar av insulindos och diet.
Pediatrisk användning
Lantus säkerhet och effektivitet har fastställts i åldersgruppen 6 till 15 år med typ 1-diabetes.
Geriatrisk användning
I kontrollerade kliniska studier som jämförde insulin glargin med NPH humant insulin, var 593 av 3890 patienter med typ 1 och typ 2-diabetes 65 år och äldre. Den enda skillnaden i säkerhet eller effektivitet i denna subpopulation jämfört med hela studiepopulationen var en förväntad högre incidens av kardiovaskulära händelser i både insulin glargin och NPH-humanbehandlad insulin patienter.
Hos äldre patienter med diabetes bör initial dosering, dosökningar och underhållsdosering vara konservativ för att undvika hypoglykemiska reaktioner. Hypoglykemi kan vara svår att känna igen hos äldre (se FÖRSIKTIGHETSÅTGÄRDER, Hypoglykemi).
topp
Negativa reaktioner
Biverkningarna som vanligtvis förknippas med Lantus inkluderar följande:
Kropp som helhet: allergiska reaktioner (se FÖRSIKTIGHETSÅTGÄRDER).
Hud och bilagor: reaktion på injektionsstället, lipodystrofi, klåda, utslag (se FÖRSIKTIGHETSÅTGÄRDER).
Annat: hypoglykemi (se VARNINGAR och FÖRSIKTIGHETSÅTGÄRDER).
I kliniska studier på vuxna patienter fanns det en högre förekomst av smärta på injektionsstället på behandlingsspråk hos Lantus-behandlade patienter (2,7%) jämfört med NPH-insulinbehandlade patienter (0,7%). Rapporteringen om smärta på injektionsstället var vanligtvis milda och ledde inte till att behandlingen avbröts. Andra reaktioner på injektionsstället som uppstod på behandlingen inträffade vid liknande händelser med både insulin glargin och NPH humant insulin.
Retinopati utvärderades i de kliniska studierna med hjälp av rapporterade biverkningar i näthinnan och fundusfotografering. Antalet biverkningar i näthinnan rapporterade för Lantus- och NPH-behandlingsgrupper var liknande för patienter med typ 1 och typ 2-diabetes. Progression av retinopati undersöktes med fundusfotografering med användning av ett graderingsprotokoll härrörande från Early Treatment Diabetic Retinopathy Study (ETDRS). I en klinisk studie där patienter med typ 2-diabetes var en skillnad i antalet personer med â-3-steg progression i ETDRS-skala under en 6-månadersperiod noterades av fundusfotografering (7,5% i Lantus-gruppen mot 2,7% i NPH behandlad grupp). Den övergripande relevansen av detta isolerade fynd kan inte fastställas på grund av det lilla antalet patienter involverade, den korta uppföljningsperioden och det faktum att detta fynd inte observerades i andra kliniska studier.
topp
Överdos
Överskott av insulin i förhållande till matintag, energiförbrukning eller båda kan leda till svår och ibland långsiktig och livshotande hypoglykemi. Milda avsnitt av hypoglykemi kan vanligtvis behandlas med orala kolhydrater. Justeringar i läkemedelsdosering, måltidsmönster eller träning kan behövas.
Mer allvarliga episoder med koma, krampanfall eller neurologiskt nedsättning kan behandlas med intramuskulär / subkutan glukagon eller koncentrerad intravenös glukos. Efter uppenbar klinisk återhämtning från hypoglykemi kan fortsatt observation och ytterligare kolhydratintag vara nödvändigt för att undvika återfall av hypoglykemi.
topp
Dosering och administrering
Lantus är en rekombinant humaninsulinanalog. Dess styrka är ungefär densamma som humant insulin. Den uppvisar en relativt konstant glukos-sänkande profil under 24 timmar som tillåter dosering en gång dagligen.
Lantus kan administreras när som helst under dagen. Lantus ska ges subkutant en gång om dagen vid samma tidpunkt varje dag. För patienter som justerar tidpunkten för dosering med Lantus, se VARNINGAR och FÖRSIKTIGHETSÅTGÄRDER, Hypoglykemi. Lantus är inte avsett för intravenös administrering (se FÖRSIKTIGHETSÅTGÄRDER). Intravenös administrering av den vanliga subkutana dosen kan leda till svår hypoglykemi. De önskade blodsockernivåerna samt doserna och tidpunkten för mediciner mot diabetes måste bestämmas individuellt. Blodglukosövervakning rekommenderas för alla patienter med diabetes. Den förlängda aktiviteten av Lantus är beroende av injektion i det subkutana utrymmet.
Som med alla insuliner måste injektionsställen inom ett injektionsområde (buk, lår eller deltoid) roteras från en injektion till nästa.
I kliniska studier fanns det ingen relevant skillnad i absorptionen av glargininsulin efter subkutan administrering av buken, deltoid eller låret. Vad gäller alla insuliner kan absorptionshastigheten, och följaktligen början och varaktigheten av verkan, påverkas av träning och andra variabler.
Lantus är inte valet insulin för behandling av diabetes ketoacidos. Intravenöst kortverkande insulin är den föredragna behandlingen.
Pediatrisk användning
Lantus kan administreras säkert till pediatriska patienter på 6 år. Administration till barn
Initiering av Lantus-terapi
I en klinisk studie med insulinöverskådade patienter med diabetes typ 2 som redan behandlats med orala antidiabetesläkemedel, startades Lantus vid en genomsnittlig dos på 10 IE en gång dagligen, och justeras därefter enligt patientens behov till en total daglig dos som sträcker sig från 2 till 100 IU.
Byt till Lantus
Om man byter från en behandlingsregim med ett mellanliggande eller långverkande insulin till ett Lime-behandlingsregime, är mängden och tidpunkten för kortverkande insulin eller snabbverkande insulinanalog eller dosen av vilket som helst oralt antidiabetesläkemedel kan behövas justeras. När patienter överfördes från NPH humaninsulin eller ultralente humant insulin till Lantus en gång dagligen, ändrades vanligtvis inte initialdosen i kliniska studier. Men när patienter överfördes från humant insulin NPH två gånger dagligen till Lantus en gång dagligen, för att minska risken för hypoglykemi, dosen (IE) reducerades vanligtvis med cirka 20% (jämfört med total daglig IU av NPH humant insulin) och justerades sedan baserat på patientens svar (ser FÖRSIKTIGHETSÅTGÄRDER, Hypoglykemi).
Ett program för nära metabolisk övervakning under medicinsk övervakning rekommenderas under överföring och under de första veckorna därefter. Mängden och tidpunkten för kortverkande insulin eller snabbverkande insulinanalog kan behöva justeras. Detta gäller särskilt för patienter med förvärvade antikroppar mot humant insulin som behöver höga insulindoser och inträffar med alla insulinanaloger. Dosjustering av Lantus och andra insuliner eller orala antidiabetesläkemedel kan behövas; till exempel om patientens tidpunkt för dosering, vikt eller livsstilsförändringar eller andra omständigheter uppstår som ökar känsligheten för hypoglykemi eller hyperglykemi (se FÖRSIKTIGHETSÅTGÄRDER, Hypoglykemi).
Dosen kan också behöva justeras vid samtidiga sjukdomar (se FÖRSIKTIGHETSÅTGÄRDER, Mellanströmförhållanden).
Förberedelser och hantering
Parenterala läkemedelsprodukter bör inspekteras visuellt före administrering när lösningen och behållaren tillåter. Lantus får endast användas om lösningen är klar och färglös utan synliga partiklar.
Blandning och utspädning: Lantus får INTE spädas eller blandas med något annat insulin eller lösning (se FÖRSIKTIGHETSÅTGÄRDER, Allmänt).
Injektionsflaska: Injektionssprutorna får inte innehålla något annat läkemedel eller rester.
Patronsystem: Om OptiClik®, insulinleveransenheten för Lantus, fungerar, kan Lantus dras från patronsystemet i en U-100-spruta och injiceras.
topp
Hur levereras
Lantus 100 enheter per ml (U-100) finns i följande paketstorlek:
10 ml injektionsflaskor (NDC 0088-2220-33)
3 ml patronsystem1, paket med 5 (NDC 0088-2220-52)
1Patronsystem är endast avsedda att användas i OptiClik® (Insulin Delivery Device)
Lagring
Oöppnat Vial / Cartridge-system
Oöppnade Lantus-injektionsflaskor och patronsystem ska förvaras i kylskåp, 2 ° C - 8 ° C. Lantus ska inte förvaras i frysen och det får inte frysas.
Kassera om den har frysts.
Öppet (i användning) Vial / Cartridge-system
Öppnade injektionsflaskor, oavsett om de är kylda, måste användas inom 28 dagar efter första användning. De måste kasseras om de inte används inom 28 dagar. Om kylning inte är möjlig kan det öppna injektionsflaskan hållas okyld i upp till 28 dagar från direkt värme och ljus, så länge temperaturen inte är högre än 30 ° C.
Det öppnade (i användning) kassettsystemet i OptiClik® ska INTE kylas utan ska hållas vid rumstemperatur (under 86 ° F [30 ° C]) borta från direkt värme och ljus. Det öppnade (i användning) patronsystemet i OptiClik® som hålls vid rumstemperatur måste kasseras efter 28 dagar. Förvara inte OptiClik®, med eller utan kassasystem, i kylskåp när som helst.
Lantus ska inte förvaras i frysen och det får inte frysas. Kassera om den har frysts.
Dessa lagringsvillkor sammanfattas i följande tabell:
| Används inte (oöppnad) Kallt |
Används inte (oöppnad) Rumstemperatur |
I användning (öppnad) (Se temperatur nedan) |
|
|---|---|---|---|
| 10 ml injektionsflaska | Fram till utgångsdatum | 28 dagar | 28 dagar Kyl eller rumstemperatur |
| 3 ml patronsystem | Fram till utgångsdatum | 28 dagar | 28 dagar Kyl eller rumstemperatur |
| 3 ml patron system infogat i OptiClik® |
28 dagar Endast rumstemperatur (Kyl inte) |
Tillverkad för distribuerad av:
sanofi-aventis U.S. LLC
Bridgewater NJ 08807
Gjord i Tyskland
www. Lantus.com
© 2006 sanofi-aventis U.S. LLC
OptiClik® är ett registrerat varumärke som tillhör sanofi-aventis U.S. LLC, Bridgewater NJ 08807
senast uppdaterad 04/2006
Lantus, insulin glargin (rDNA-ursprung), patientinformation (på vanligt engelska)
Detaljerad information om tecken, symtom, orsaker, behandling av diabetes
Informationen i denna monografi är inte avsedd att täcka alla möjliga användningar, anvisningar, försiktighetsåtgärder, läkemedelsinteraktioner eller negativa effekter. Denna information är generaliserad och är inte avsedd som specifik medicinsk rådgivning. Om du har frågor om läkemedlen du tar eller vill ha mer information, kontakta din läkare, apotekspersonal eller sjuksköterska.
tillbaka till: Bläddra bland alla mediciner för diabetes



